信息系統在行政審批業務中的廣泛應用,要求企業相關人員要熟悉政府審批系統及了解信息系統的變化。就醫療器械注冊事項而言,浙江省第二類醫療器械注冊指定檢驗辦理因為涉及到兩個平臺,流程是較為復雜。
信息系統在行政審批業務中的廣泛應用,要求企業相關人員要熟悉政府審批系統及了解信息系統的變化。就醫療器械注冊事項而言,浙江省第二類醫療器械注冊指定檢驗辦理因為涉及到兩個平臺,流程是較為復雜。

一、為什么要辦理第二類醫療器械注冊指定檢驗?
1.國家法律依據:
(一)《醫療器械注冊管理辦法》第十八條
醫療器械檢驗機構應當具有醫療器械檢驗資質、在其承檢范圍內進行檢驗,并對申請人提交的產品技術要求進行預評價。預評價意見隨注冊檢驗報告一同出具給申請人。尚未列入醫療器械檢驗機構承檢范圍的醫療器械,由相應的注冊審批部門指定有能力的檢驗機構進行檢驗。
(二)《體外診斷試劑注冊管理辦法》第二十六條
醫療器械檢驗機構應當具有醫療器械檢驗資質、在其承檢范圍內進行檢驗,并對申請人提交的產品技術要求進行預評價。預評價意見隨注冊檢驗報告一同出具給申請人。尚未列入醫療器械檢驗機構承檢范圍的產品,由相應的注冊審批部門指定有能力的檢驗機構進行檢驗。
(三)《醫療器械注冊指定檢驗工作管理規定》第五條
指定檢驗申請人向相應的食品藥品監督管理部門提出指定檢驗申請,并提交以下資料:
(一)醫療器械注冊指定檢驗申請;
(二)待檢產品的技術要求;
(三)擬指定的醫療器械檢驗機構出具的檢驗能力證明。
2.受理條件:
(一)明確待檢產品的管理類別為第二類醫療器械。
(二)待檢產品不在任何一家經資質認定的醫療器械檢驗機構承檢范圍內。
二、第二類醫療器械注冊指定檢驗申報材料:
1.醫療器械注冊指定檢驗申請表;
2.待檢產品的技術要求掃描件;
3.擬指定的醫療器械檢驗機構出具的檢驗能力聲明掃描件;
4.授權委托書和經辦人身份證復印件掃描件。
三、第二類醫療器械注冊指定檢驗辦理流程:
1.向擬指定的醫療器械檢驗機構申請檢驗能力聲明文件,取得檢驗機構同意;
2.向浙江省藥品監督管理局(浙江省政務服務網)申請第二類醫療器械注冊指定檢驗;
3.在浙江省藥品監督管理局官網下載《第二類醫療器械指定檢驗證書》。
四、第二類醫療器械注冊指定檢驗辦理常見問題:
1.醫療器械注冊指定檢驗的辦理流程設計到檢驗院和省藥監局,要注意申請的先后順序;先檢驗院,再藥監局。
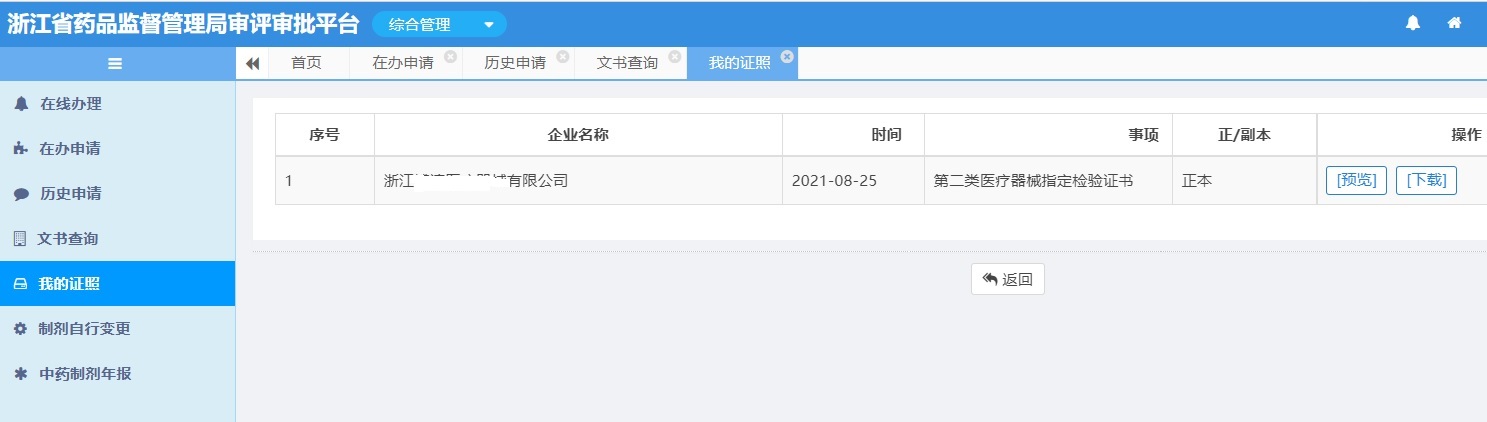
2.由于藥監局辦理第二類醫療器械注冊指定檢驗審批涉及到兩個平臺,即浙江省政務服務網和浙江省藥品監督管理局官網,大家要記得是在浙江政務服務網申請,而后在浙江省藥品監督管理局官網下載證書。下載證書的地方也不是很好找到,我放個圖片,方便大家了解。
圖1.第二類醫療器械注冊指定檢驗證書下載處
任何疑問,歡迎您隨時方便與杭州證標客醫藥技術咨詢有限公司葉工聯系,聯系電話:18058734169,微信同。