跟大家一起來看浙江省藥監局近期公開的創新醫療器械(3D電子胸腹腔鏡)審評報告,一起來學習和了解浙江省申請創新醫療器械有什么要求。
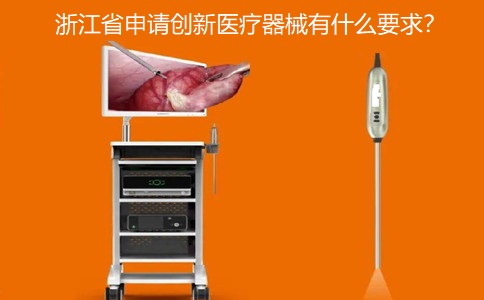
浙江省藥監局公開創新醫療器械(3D電子胸腹腔鏡)審評報告:
一、基本情況
醫療器械產品主冊技術審評報告
產品中文名稱: 3D電子胸腹腔鏡
產品管理類別:第二類
申請人名稱:賽諾微醫療科技(浙江)有限公司
二、產品審評摘要
1.產品概述
(一)產品結構及組成
.產品由保護窗片、鏡管前端(內含LED光源照明組件和攝像組件)、鏡管后端、手柄、按鍵和線纜組成。
(二)產品適用范圍
產品與電子內窺鏡圖像處理器(EVS200) 配合使用,用于胸腔和腹腔的觀察成像。
(三)型號/規格
LPS31000、LPS31030
(四)工作原理
光源發出的光經過照明透鏡照射到組織上,頭端部的圖像傳感器(CMOS) 將接收到的兩路有視差的組織反射光信號轉換為電信號,通過電纜線傳輸到圖像處理裝置,圖像處理裝置接受來自內窺鏡的圖像信號并轉換成3D影像信號,最終呈現在3D顯示器上,3D顯示器將兩路有視差的圖像信息分別發送至觀察者的左右眼,通過人的大腦形成立體視覺,從而產生手術需要的縱深感。
2.臨床前研究摘要
(一)產品性能研究
性能指標參考相關國家、行業標準制定,包括: GB 9706. 1-2007、GB 9706. 19-2000、YY 0068. 1-2008、YY 0068. 2-2008、YY 0068. 3-2008、YY 0068. 4 -2009、YY/T 1587-2018、 YY 0505-2012等。根據GB/T 14710-2009確定了環境試驗要求。
(二)生物相容性
依據GB/T 16886系列標準提交生物相容性評價,包含與組織直接接觸材料的生物學試驗報告。該報告由具有資質的醫療器械檢驗機構出具,檢驗項目為體外細胞毒性試驗、皮內反應試驗、皮膚致敏試驗,檢驗結果符合要求。
(三)產品有效期和包裝
參考《有源醫療器械使用期限注冊技術審查指導原則》要求提交了產品使用期限的研究資料;提交在宣稱的有效期內以及運輸儲存條件下保持包裝完整性的研究資料。
(四)軟件研究
產品包含數據采集器嵌入式軟件,軟件主要功能包括光源亮度調節功能、拍攝和錄像功能、圖像參數設置功能等;依據《醫療器械軟件注冊技術審查指導原則》要求提交軟件研究資料,包括軟件描述文檔和軟件版本命名規則真實性聲明,證明軟件設計開發過程規范可控,剩余風險均可接受。
(五)有源設備安全性指標
符合GB 9706. 1-2007. GB 9706. 19-2000、YY 0505-2012 要求。
三、臨床評價摘要
按照《醫療器械臨床評價技術指導原則》要求,通過同品種醫療器械臨床數據進行分析評價。
選取已上市的3D高清電子腹腔鏡(注冊證號:國械注進20163062452)作為對比產品。提交基本原理、結構組成、適用
范圍等方面的對比分析,提供性能參數等方面的測試對比報告、差異部分安全有效性分析報告、動物實驗報告、臨床文獻及同品種產品臨床數據等證明產品的安全、有效性。
四、風險分析及說明書提示
(一)風險分析
申請人根據YY/T 0316-2016 《醫療器械風險管理對醫療器械的應用》及其內部質量管理體系規定執行風險管理相關活
動,對目前已知及可預測風險采取了風險控制措施,經綜合評價,認為該產品在正常使用條件下,可達到預期性能;與預期受益相比較,綜合剩余風險可接受。
(二)警示及注意事項
1.本產品使用者必須是具有特定技術和外科手術訓練的合格醫療專業人員。
2.3D電子腹腔鏡不適用于對照液、硬化治療液和麻醉劑等強腐蝕性液體。
3.3D電子胸腹腔鏡與其他設備之間可能存在潛在的電磁干擾。
4.3D電子胸腹腔鏡與電子內窺鏡圖像處理器需要通過特制的連接端口進行連接,3D電子胸腹腔鏡僅可與由賽諾微聲明可以配合使用的電子內窺鏡圖像處理器連接。
5.視野范圍外的應用部分,存在意外損傷組織和損害附件的風險。使用期間,應始終保持活性電極和3D電子胸腹腔鏡的應用部分以及其它向標靶位置發射能量的設備處于視野范圍內。
6.對裝有心臟起搏器的患者,必須確保3D電子胸腹腔鏡的近端(即:于患者相隔最遠的一端)與起搏器之間的距離至少為
2cm。設備的手柄處會產生一個磁場,這樣的磁場可能導致心臟起搏器或其它電子設施發生故障。
7.不得使用潮濕的電纜。
8.3D電子胸腹腔鏡連接器的金屬部件與電子內窺鏡圖像處理器的保護殼之間有電氣連接。使用期間,確保這些金屬部件不會接觸到接地電位。
(三)禁忌癥
1.說明書中“適用范圍”以外的病例;
2.禁止將本產品與心臟直接接觸使用;
3.其他禁忌癥需要手術醫生根據特定手術適用的專業標準
加以判斷。
五、綜合評價意見
該申報產品屬《第二類創新醫療器械特別審批程序(試行)》(浙食藥監規(2016] 2號)審批項目,創新審查受理
號:器械20212554。 經審評符合技術審查標準,建議準予注冊。
標簽:申請創新醫療器械有什么要求