- 聯系我們

聯系電話:0571-86198618手機: 18058734169 (微信同)手機:18868735317(微信同)周一至周日 8:00~22:00
在線客服周一至周日 8:00~22:00
-
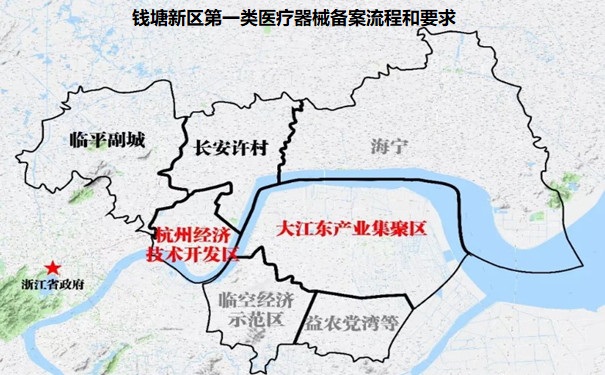
錢塘新區第一類醫療器械備案流程和要求 錢塘新區是杭州行政區劃調整后形成的新區,新區有其獨特的定位,并在醫療器械產業招商方面做了許多卓有成效的工作,越來越多醫療器械器械落戶錢塘新區。本文為大家介紹錢塘新區第一類醫療器械備案流程?和要求。 時間:2023-3-5 19:20:51 瀏覽量:981
-
有源醫療器械注冊產品增加規格型號,是否必須進行檢測? 對于有源醫療器械注冊產品來說,技術迭代和需求變化是高頻發生的事情,而醫療器械注冊及監管法規要求生產的產品與注冊申報的保持一致,當已取得醫療器械注冊證的產品增加新的規格型號時,是否必須進行檢測?一起看本文。 時間:2023-3-5 18:53:42 瀏覽量:1375

-
湖南創面敷料類醫療器械產品注冊要點 過去5年是湖南省醫療器械產業快速發展的五年,醫療器械注冊產品和獲證企業數量增長迅猛,取得了許多許多了不起的業績。過去5年,也是敷料類產品光彩奪目、跌宕起伏的五年,因為敷料類產品廣泛的臨床應用場景和巨大的消費市場,也因為敷料類產品組成結構及作用機理的復雜及監管風險。本文為大家帶來湖南省藥監局有關創面敷料類醫療器械產品注冊事項答疑,一起來學習。 時間:2023-3-4 0:00:00 瀏覽量:1157

-
常規超高分子量聚乙烯單髁膝關節假體的襯墊厚度要求 單髁膝關節假體在我做屬于第三類醫療器械注冊?產品,近日,國家藥監局發布醫療器械注冊答疑事項,明晰常規超高分子量聚乙烯單髁膝關節假體的襯墊厚度要求。一起看正文。 時間:2023-3-2 22:30:17 瀏覽量:1030

-
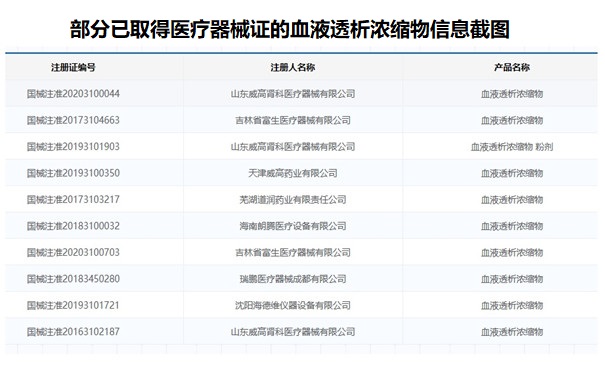
血液透析濃縮物注冊產品的A劑是否可以按成分分別包裝? 血液透析濃縮物通常由A液、B粉兩部分組成。A液是由氯化鈉、氯化鉀、氯化鈣、氯化鎂、冰醋酸、葡萄糖組成。B粉由碳酸氫鈉組成。血液透析濃縮物在我國屬于第三類醫療器械注冊?產品,適用于急、慢性腎功能衰竭患者進行血液透析治療。 時間:2023-3-2 0:00:00 瀏覽量:1215
-
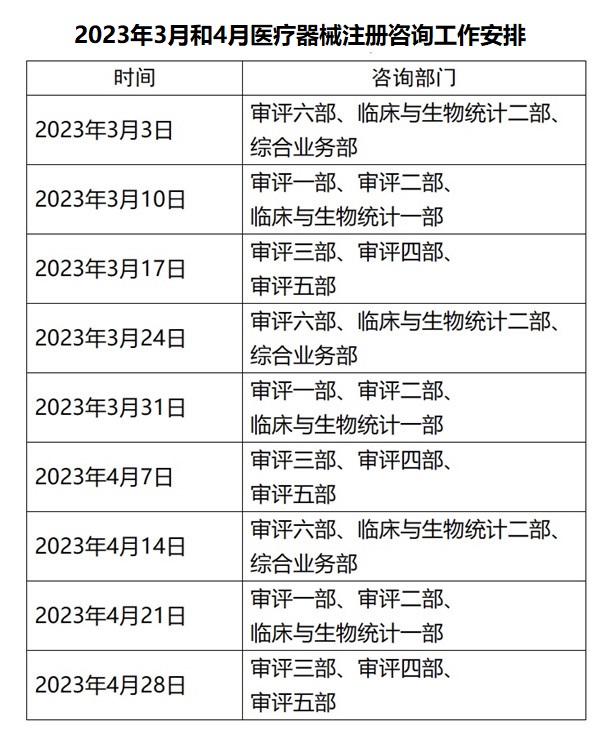
2023年3月和4月藥監總局醫療器械注冊咨詢工作安排 為做好醫療器械注冊受理前技術問題咨詢工作,指導行政相對人安排咨詢時間,保證咨詢工作質量,近日藥監總局發布2023年3月和4月藥監總局醫療器械注冊咨詢工作安排 時間:2023-2-27 21:58:48 瀏覽量:1064
-
2023年1月上海醫療器械注冊審評用時情況 上海第二類醫療器械注冊要多少時間是多數醫療器械注冊企業關心的核心問題之一,據上海市藥監局公布的數據,2023年1月,上海市第二類醫療器械注冊審評平均用時56個工作日,第二類醫療器械變更注冊審評平均用時41個工作日,第二類醫療器械延續注冊平均用時23個工作日。 時間:2023-2-27 21:50:16 瀏覽量:1400

-
麗水市第一類醫療器械產品備案流程和要求 盡管麗水市醫療器械產業相比浙江其它地區沒有那么大的體量,但近幾年仍然有不少麗水企業進入醫療器械行業,本文為大家科普麗水市第一類醫療器械產品備案?流程和要求。 時間:2023-2-24 12:52:25 瀏覽量:933

-
上海第二類醫療器械注冊電子申報高頻問題 來自上海市藥監局的官方消息,為方便企業辦理醫療器械電子申報相關業務,上海市器審中心受理部整理了部分上海第二類醫療器械注冊電子申報高頻問題,涉及現場檢查不合格項整改資料報送、電子簽章、輔助工具使用等,以一問一答的形式幫助辦事人員準確高效地辦理相關業務事項。 時間:2023-2-22 16:41:22 瀏覽量:976

-
醫療器械注冊或生產企業產品留樣有什么要求 對于醫療器械注冊或是醫療器械生產企業來說,做好產品留樣不僅僅是為滿足法規或行業最佳實踐要求,此外,留樣在追溯性及控制爭議和處罰方面也發揮著不可忽視的作用。 時間:2023-2-22 16:31:34 瀏覽量:1283

-
無菌檢驗員線上培訓課程上線了 經過前后兩年的線下無菌檢驗員培訓、微生物檢驗員培訓經驗積累及沉淀,經過我們專業無菌檢驗員培訓團隊超過六個月的拍攝、錄制、打磨,以及來自浙江省醫療器械檢驗研究院、無菌檢驗設備廠家、無菌檢驗耗材廠家的大力支持和幫助下,以及我們歷屆學員的努力學習、良好支持和反饋,醫療器械實訓中心原創的2020版《中國藥典》無菌微生物檢驗員線上培訓課程終于上線 時間:2023-2-22 16:02:45 瀏覽量:1190

-
甘肅第二、第三類醫療器械生產許可證辦理流程和要求 與浙江醫療器械生產許可證辦理審批不同的是,甘肅第二、第三類醫療器械生產許可證均屬于甘肅省藥品監督管理局經辦項目,一起來了解甘肅第二、第三類醫療器械生產許可證辦理流程和要求。 時間:2023-2-21 18:16:31 瀏覽量:1267

-
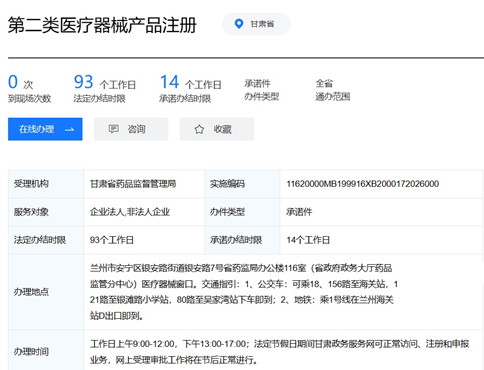
甘肅第二類醫療器械產品注冊流程和要求 甘肅下轄12個地級市、2個自治州,是西北地區經濟和政治中心之一,也有非常好的醫療產業基礎,正好因為工作出差到甘肅武威,寫個文章為大家科普有關甘肅第二類醫療器械產品注冊流程?和要求。 時間:2023-2-21 17:12:08 瀏覽量:1079
-
甘肅醫療機構制劑注冊流程和要求 《藥品管理法》第七十六條規定:醫療機構配制的制劑,應當是本單位臨床需要而市場上沒有供應的品種,并應當經所在地省、自治區、直轄市人民政府藥品監督管理部門批準;但是,法律對配制中藥制劑另有規定的除外。醫療機構配制的制劑應當按照規定進行質量檢驗;合格的,憑醫師處方在本單位使用。本文為大家介紹甘肅醫療機構制劑注冊流程和要求。 時間:2023-2-21 16:59:36 瀏覽量:1233
-
國家局發布神經和心血管介入導管類醫療器械注冊答疑1項 自2017年左右開始,我國醫療器械研發與制造逐步從常規醫療器械、從低風險醫療器械,到高風險醫療器械、創新醫療器械研制,越來越多的國產神經和心血管介入導管類醫療器械注冊?產品獲批上市。近日,國家局發布神經和心血管介入導管類醫療器械注冊答疑1項,一起來了解。 時間:2023-2-20 10:22:59 瀏覽量:1080
-
杭州藥包材登記流程和資料要求 盡管杭州最被大家熟知的名片是互聯網之都和世界聞名的西湖,但也有許多行業和產業在已有產業的引領下,悄然成長,比如,醫藥產業,醫療器械產業,及藥包材產業。本文為大家科普杭州藥包材登記流程和資料要求。 時間:2023-2-16 20:45:18 瀏覽量:1108

-
杭州第一類醫療器械備案時,有關生物學檢測事項如何考量 第一類醫療器械備案項目屬于市級市場監督管理局辦理事項,各地辦理要求和流程略有差異,本文問大家介紹杭州第一類醫療器械備案時,有關生物學檢測事項如何考量。 時間:2023-2-16 20:31:53 瀏覽量:945
-
杭州體外診斷試劑銷售辦理醫療器械經營許可證的要求 醫療器械經營許可證辦理事項因在各地不同地區、各個擬經營醫療器械類別和特性不同,辦理的要求都存在差異,本文為大家科普杭州體外診斷試劑銷售辦理醫療器械經營許可證?的要求。 時間:2023-2-16 20:15:44 瀏覽量:900

-
國家局發布血液凈化醫療器械注冊產品相關答疑1項 近日,國家局發布血液凈化醫療器械注冊產品相關答疑1項,針對腎功能衰竭患者的血液凈化產品生物學評價應如何考慮,一起來關注。 時間:2023-2-14 20:33:40 瀏覽量:934

-
產前遺傳學檢測技術簡介 《中國出生缺陷防治報告(2012)》顯示,我國出生缺陷發生率在5.6%左右,每年新增出生缺陷數約90萬例。產前遺傳病檢查通常使用產前遺傳病檢測設備及相關配套的體外診斷試劑注冊產品,一般包括全基因組測序、通過基因芯片檢測染色體、進行單基因疾病檢測等項目。 時間:2023-2-14 20:11:56 瀏覽量:1269

